“CRISPR-Cas sistēmas” baktērijās un vīrusos identificē un iznīcina invazīvās vīrusu sekvences. Tā ir baktēriju un arheālu imūnsistēma aizsardzībai pret vīrusu infekcijām. 2012. gadā CRISPR-Cas sistēma tika atzīta par a Genoma rediģēšanas rīks. Kopš tā laika ir izstrādāts plašs CRISPR-Cas sistēmu klāsts, un tās ir atradušas pielietojumu tādās jomās kā gēnu terapija, diagnostika, pētniecība un ražas uzlabošana. Tomēr pašlaik pieejamām CRISPR-Cas sistēmām ir ierobežota klīniskā izmantošana, jo bieži notiek ārpusmērķa rediģēšana, neparedzētas DNS mutācijas un iedzimtas problēmas. Pētnieki nesen ziņoja par jaunu CRISPR-Cas sistēmu, kas var mērķēt un iznīcināt mRNS un proteīni precīzāk saistīti ar dažādām ģenētiskām slimībām bez nevēlamas ietekmes un pārmantojamām problēmām. Ar nosaukumu Craspase tā ir pirmā CRISPR-Cas sistēma, kas tiek parādīta proteīns rediģēšanas funkcija. Tā ir arī pirmā sistēma, kas var rediģēt gan RNS, gan proteīns. Tā kā Craspase pārvar daudzus esošo CRISPR-Cas sistēmu ierobežojumus, tai ir potenciāls revolucionizēt gēnu terapiju, diagnostiku un uzraudzību, biomedicīnas izpēti un ražas uzlabošanu.
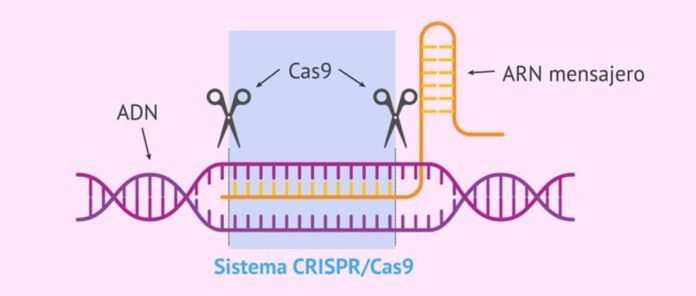
“CRISPR-Cas sistēma” ir dabiska baktēriju un arheju imūnsistēma pret vīrusu infekcijām, kas identificē, saistās un degradē vīrusa gēna sekvences, lai aizsargātu. Tas sastāv no divām daļām – baktēriju RNS, kas pārrakstīta no vīrusa gēna, kas iekļauts baktēriju genomā pēc pirmās inficēšanās (ko sauc par CRISPR, tas identificē iebrūkošo vīrusu gēnu mērķa sekvences) un ar to saistītā iznīcinātāja. proteīns ar nosaukumu “CRISPR saistīts proteīns (Cas)”, kas saista un noārda identificētās sekvences vīrusa gēnā, lai aizsargātu baktērijas pret vīrusiem.
CRISPER apzīmē "grupētus regulāri interstarpus īsus palindromiskus atkārtojumus". Tā ir transkribēta baktēriju RNS, ko raksturo palindromiski atkārtojumi.
Palindromiskie atkārtojumi (CRISPR) pirmo reizi tika atklāti sekvencēs E. coli 1987. gadā Fransisko Mohika novēroja līdzīgas struktūras arhejās, un tieši viņš pirmais uzskatīja, ka tās ir baktēriju un arheju imūnsistēmas daļa. 1995. gadā pirmo reizi eksperimentāli tika pierādīts, ka baktēriju un arheju imūnsistēmas mērķis bija sveša DNS, nevis mRNS. Vīrusu sekvenču identifikācijas un degradācijas mehānisms liecināja, ka šādas sistēmas varētu izmantot kā līdzekli genoma rediģēšana. Kopš 2012. gadā, kad CRISPR–Cas sistēma tika atzīta par genoma rediģēšanas rīku, tā ir nogājusi ļoti garu ceļu kā stabils standarts. gēnu rediģēšana sistēmu un ir atradis plašu pielietojumu klāstu biomedicīnā, lauksaimniecībā, farmācijas nozarēs, tostarp klīniskajā gēnu terapijā1,2.
Plašs CRISPR-Cas sistēmas jau ir identificētas un pašlaik ir pieejamas DNS/RNS sekvenču uzraudzībai un rediģēšanai pētniecībai, zāļu skrīningam, diagnostikai un ārstēšanai. Pašreizējās CRISPR/Cas sistēmas ir sadalītas 2 klasēs (1. un 2. klase) un sešos veidos (I līdz XI tips). 1. klases sistēmām ir vairākas Cas proteīni kurām jāveido funkcionāls komplekss, lai saistītu un iedarbotos uz to mērķiem. No otras puses, 2. klases sistēmām ir tikai viena liela Cas proteīns mērķa sekvenču saistīšanai un degradēšanai, kas padara 2. klases sistēmas vieglāk lietojamas. Parasti izmantotās 2. klases sistēmas ir Cas 9 II tips, Cas13 VI tips un Cas12 V tips. Šīm sistēmām var būt nevēlama blakusiedarbība, ti, ietekme ārpus mērķa un citotoksicitāte.3,5.
Gēnu terapijas pamatojoties uz pašreizējām CRISPR-Cas sistēmām, ir ierobežota klīniskā izmantošana, jo bieži notiek ārpusmērķa rediģēšana, negaidītas DNS mutācijas, tostarp lielas DNS fragmentu dzēšanas un lieli DNS strukturālie varianti gan mērķa, gan ārpus mērķa vietās, kas izraisa šūnu nāvi. un citas iedzimtas problēmas.
Craspase (vai CRISPR vadīta kaspāze)
Pētnieki nesen ziņoja par jaunu CRISPER-Cas sistēmu, kas ir 2. klases III-E tipa Cas7-11 sistēma, kas saistīta ar kaspāzei līdzīgu sistēmu. proteīns tāpēc nosaukts Craspase vai CRISPR vadīta kaspāze 5 (Kaspāzes ir cisteīna proteāzes, kurām ir galvenā loma apoptozē, sadalot šūnu struktūras). Tam ir potenciāls pielietojums tādās jomās kā gēnu terapija un diagnostika. Craspase ir RNS vadīta un mērķēta uz RNS, un tā nav saistīta ar DNS sekvencēm. Tas var mērķēt un iznīcināt mRNS un proteīni precīzāk saistīti ar dažādām ģenētiskām slimībām bez nevēlamas ietekmes. Tādējādi ar slimībām saistīto gēnu likvidēšana ir iespējama, šķeļot mRNS vai olbaltumvielu līmenī. Turklāt, ja tas ir saistīts ar noteiktu enzīmu, Craspase var izmantot arī proteīnu funkciju modificēšanai. Kad tās RNāzes un proteāzes funkcijas tiek noņemtas, Craspase tiek deaktivizēta (dCraspase). Tam nav griešanas funkcijas, bet tas saistās ar RNS un olbaltumvielu sekvencēm. Tāpēc dCraspase var izmantot diagnostikā un attēlveidošanā, lai uzraudzītu un diagnosticētu slimības vai vīrusus.
Craspase ir pirmā CRISPR-Cas sistēma, kas parāda olbaltumvielu rediģēšanas funkciju. Tā ir arī pirmā sistēma, kas var rediģēt gan RNS, gan proteīnu. Tās gēnu rediģēšana funkcija rada minimālus ārpusmērķa efektus un bez pārmantojamām problēmām. Tādējādi Craspase, visticamāk, ir drošāka klīniskā lietošanā un terapijā nekā citas pašlaik pieejamās CRISPR-Cas sistēmas. 4,5.
Tā kā Craspase pārvar daudzus esošo CRISPR-Cas sistēmu ierobežojumus, tai ir potenciāls revolucionizēt gēnu terapiju, diagnostiku un uzraudzību, biomedicīnas izpēti un ražas uzlabošanu. Ir nepieciešams vairāk pētījumu, lai izstrādātu uzticamu piegādes sistēmu, lai precīzi mērķētu uz slimību izraisošiem gēniem šūnās, pirms tiek pierādīta drošība un efektivitāte klīniskajos pētījumos.
***
Norādes:
- Gostimskaya, I. CRISPR–Cas9: tās atklāšanas vēsture un tās izmantošanas ētiskie apsvērumi genoma rediģēšanā. Biochemistry Moscow 87, 777–788 (2022). https://doi.org/10.1134/S0006297922080090
- Čao Li un citi 2022. Aprēķinu rīki un resursi CRISPR/Cas genoma rediģēšanai. Genomika, proteomika un bioinformātika. Pieejams tiešsaistē 24. gada 2022. martā. DOI: https://doi.org/10.1016/j.gpb.2022.02.006
- van Beljouw, SPB, Sanders, J., Rodríguez-Molina, A. et al. RNS mērķauditorijas CRISPR-Cas sistēmas. Nat Rev Microbiol 21, 21–34 (2023). https://doi.org/10.1038/s41579-022-00793-y
- Chunyi Hu un citi 2022. gads. Craspase ir CRISPR RNS vadīta, RNS aktivēta proteāze. Zinātne. 25. gada 2022. augusts. 377. sēj., 6612. izdevums. 1278.–1285. lpp. DOI: https://doi.org/10.1126/science.add5064
- Huo, G., Shepherd, J. & Pan, X. Craspase: jauns CRISPR/Cas divu gēnu redaktors. Functional & Integrative Genomics 23, 98 (2023). Publicēts: 23. gada 2023. martā. DOI: https://doi.org/10.1007/s10142-023-01024-0
***